¡Hola!
¿Qué tal estás? Hoy vamos a comenzar con el tema de termodinámica, en concreto nos vamos a centrar en el primer principio de la termodinámica.
Los puntos que vamos a tratar son:
Conceptos previos
La termodinámica es la ciencia que estudia los cambios de energía que tienen lugar enlos procesos físicos y químicos. En toda reacción química se produce una absorción o un desprendimiento de energía, generalmente calorífica. En concreto, la termodinámica clásica estudia la variación de las variables de un sistema entre dos estados de equilibrio, uno inicial y otro final.
El sistema es la parte del universo sobre la que se centra el estudio termodinámico y al resto del universo se le llama entorno. El límite entre el sistema y su entorno se le denomina pared.
La pared puede ser:
- Adiabática: No deja pasar el calor.
- Conductora: Sí deja pasar el calor.
- Rígida: Mantiene constante el volumen del sistema.
Los sistemas pueden ser:
- Abiertos: pueden intercambiar materia y energía con el entorno.
- Cerrados: pueden intercambiar energía pero no materia con el entorno.
- Aislados: no pueden intercambiar ni materia ni energía con el entorno.
Las variables termodinámicas son las magnitudes que determinan el estado de
un sistema. Pueden ser:
- Intensivas: No dependen de la cantidad de materia del sistema y se pueden determinar en un punto cualquiera del sistema (P, T, concentración, etc)
- Extensivas: Dependen de la cantidad de materia del sistema y se extienden a todo el sistema (m, V, S, U, etc).
Una función de estado es una variable termodinámica que sólo depende del estado inicial y final del sistema, sin importar el camino que ha seguido para llegar de un punto a otro. ( entalpía, energía interna, entropía (S), Energía libre de Gibbs. etc)
Un Sistema está en equilibrio si las variables que definen el estado del sistema no varían con el tiempo.
Calor y trabajo
El intercambio de energía entre un sistema y su entorno se puede dar en forma de calor (Q) y de trabajo (W). La energía es una función de estado, sin embargo, el calor y el trabajo no, éstos son energía en tránsito.
Calor
Es la energía térmica intercambiada de forma espontánea o natural entre dos cuerpos (o entre un sistema y su entorno) que se encuentran a diferente temperatura. Se transfiere del que tiene más temperatura al que tiene menos, hasta que se alcanza el equilibrio térmico.
Se calcula: ![]()
Donde Ce es el calor específico, la cantidad de calor que hay que suministrar a 1 g de sustancia para que aumente su temperatura 1 ºC, m es la masa y ∆T es la diferencia de temperatura.
Signo del calor:
- Q>0: si ∆T>0, es decir, si aumenta la temperatura (calor absorbido)
- Q<0: si ∆T<0, es decir, si disminuye la temperatura (calor cedido)
Trabajo
Se define como la transmisión de energía debido a la acción de una fuerza que lleva consigo un desplazamiento o un cambio de volumen. En química nos interesa el trabajo de espansión-compresión que se asocian a cambios de volumen que puede experimentar un sistema.
Se calcula: ![]()
Donde P es la presión y ∆V es la variación de volumen.
Signos del trabajo:
- W>0: si ∆V<0, es decir, si disminuye el volumen (trabajo de compresión realizado por el entorno sobre el sistema)
- W<0: si ∆V>0, es decir, si aumenta el volumen (trabajo de expansión realizado por el sistema)
Lo que entra al sistema (Q o W) provoca un aumento de su energía interna y se le asigna signo + , mientras que lo que sale, provoca una disminución de energía interna y se considera con signo -.
Unidad de energía, calor y trabajo: Según el Sistema Internacional (SI) es el julio. Aunque otra unidad que también se emplea mucho son las calorías: 1 cal= 4,184 J
Primer principio de la termodinámica
La energía interna de un sistema aumenta cuando el sistema absorbe calor o soporta un trabajo.
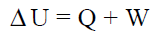
Donde la energía interna (U) es una función de estado extensiva que representa la energía total almacenada en un sistema asociada a la estructura del mismo y es la suma de las energías (cinética, potencial) de todas las partículas que conforman el sistema. Como es una función de estado, sólo depende del estado inicial y final, no del camino recorrido entre uno y otro.
Este primer principio se corresponde con el principio de la conservación de la energía:
“la energía del Universo (sistema más entorno) permanece constante” a un sistema
cerrado.
Casos particulares:
- Transformación a volumen constante (V=cte):
Si ∆V=0–> W=0–> ![]()
El calor absorbido o desprendido por el sistema a volumen constante es igual a la variación de energía interna del sistema.
- Transformación a presión constante (P=cte):
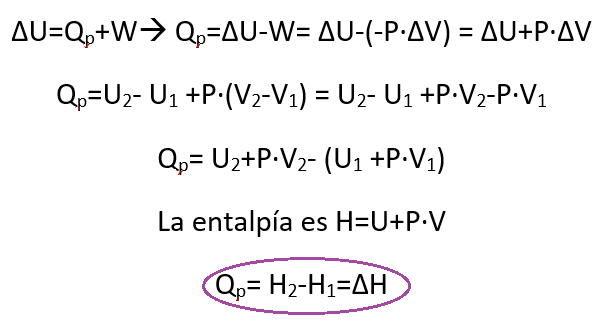
El calor absorbido o desprendido por el sistema a presión constante es igual a la variación de la entalpía del sistema.
Las magnitudes ∆H(Qp) y ∆U(Qv) se relacionan mediante:
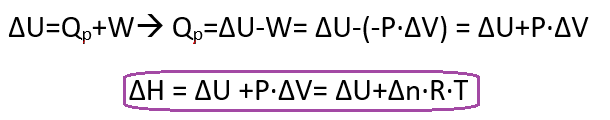
Siendo ∆n el incremento de moles gaseosos en la reacción.
Problemas resueltos



